非侵襲的なイメージング法により、生体組織へのより深い浸透が可能になります
高出力レーザーを使用するこの新しい方法は、生物学者が体の免疫応答を研究し、新薬を開発するのに役立つ可能性があります。アダム・シーウェ | MITニュース
発行日:2024年12月11日
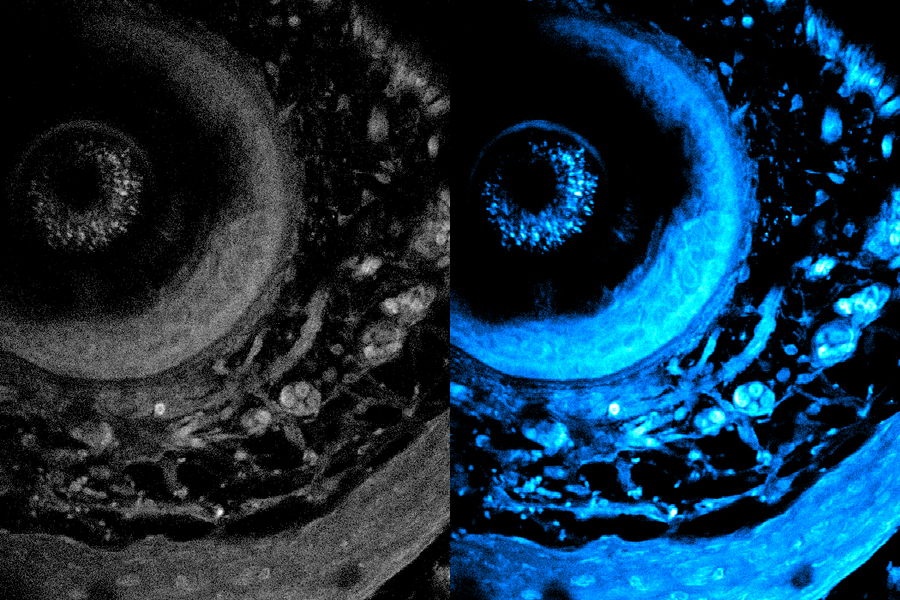
キャプション:この新しい技術により、レーザー光は生体組織のより深くまで浸透し、生体システムのさまざまな層の細胞のより鮮明な画像を取得できます。左側が初期画像で、右側が新しい手法を使用して最適化された画像です。
信用:クレジット:研究者提供
メタボリックイメージングは、臨床医や科学者がレーザー光を使用して生細胞を研究できる非侵襲的な方法であり、疾患の進行と治療反応の評価に役立ちます。
しかし、光は生体組織を透過すると散乱するため、透過できる深度が制限され、撮影された画像の解像度が妨げられます。
現在、MITの研究者は、代謝イメージングの通常の深度制限を2倍以上にする新しい技術を開発しました。また、この技術により、イメージング速度が向上し、より豊かで詳細な画像が得られます。
この新しい手法では、組織を切断したり、染料で染色したりするなど、組織の前処理は必要ありません。代わりに、特殊なレーザーが組織の奥深くまで照射され、細胞や組織内の特定のユニークな分子が光を放出します。これにより、組織を改変する必要がなくなり、その構造と機能をより自然かつ正確に表現することができます。
研究者たちは、深部組織用のレーザー光を適応的にカスタマイズすることでこれを達成しました。最近開発されたファイバーシェイパーを使用して、光の色とパルスを調整して、光が組織の奥深くまで移動するにつれて散乱を最小限に抑え、信号を最大化することができます。これにより、生体組織のより深くまで見ることができ、より鮮明な画像を得ることができます。
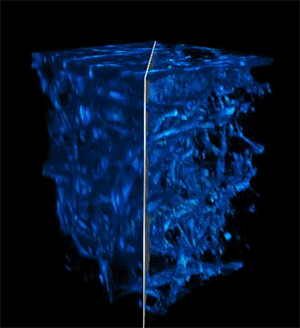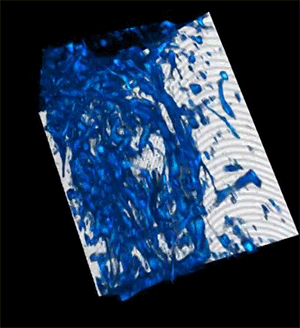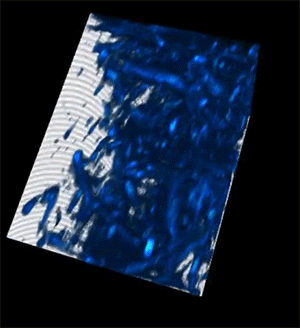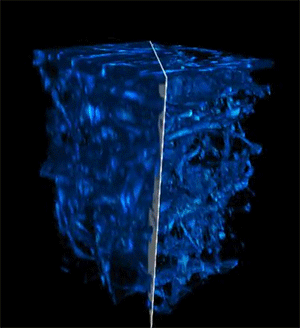
クレジット:研究者提供
深い浸透深度、高速、高解像度により、この方法は、がん研究、組織工学、創薬、免疫応答研究などの要求の厳しいイメージングアプリケーションに特に適しています。
「この研究は、ラベルフリーの代謝イメージングの深さの浸透性の点で大幅な改善を示しています。これは、生体システムの深部にある代謝ダイナミクスを研究し、探求するための新たな道を開きます」と、電子工学研究所のメンバーであり、このイメージング技術に関する論文の上級著者である電気工学およびコンピューターサイエンス学部(EECS)の助教授であるSixian Youは述べています。
彼女は、EECSの大学院生である筆頭著者のKunzan Liuが論文に参加しています。Tong Qiu、MITポスドク。EECSの大学院生であるHonghao Cao。ファン・ワン、脳および認知科学の教授。ロジャー・カム、セシル・アンド・アイダ・グリーンの生物工学および機械工学の著名な教授。リンダ・グリフィス、工学部生物工学科の教育イノベーション教授。
レーザー集束
この新しい方法は、ラベルフリーイメージングのカテゴリーに分類され、組織を事前に染色しません。染色はコントラストを生み出し、臨床生物学者が細胞核とタンパク質をよりよく見るのに役立ちます。しかし、染色には通常、生物学者がサンプルを切片化してスライスする必要があり、このプロセスにより組織が死滅し、生細胞の動的プロセスを研究することが不可能になることがよくあります。
ラベルフリーイメージング技術では、研究者はレーザーを使用して細胞内の特定の分子を照射し、さまざまな色の光を放出して、さまざまな分子内容物や細胞構造を明らかにします。しかし、深部組織イメージングのために、特定の波長と高品質のパルスを持つ理想的なレーザー光を生成することは困難でした。
研究者たちは、この制限を克服するための新しいアプローチを開発しました。彼らは、大量の電力を伝送できる光ファイバーの一種であるマルチモードファイバーを「ファイバーシェイパー」と呼ばれるコンパクトなデバイスと結合します。このシェイパーにより、ファイバーの形状を適応的に変更することにより、光の伝播を正確に調整できます。ファイバーを曲げると、レーザーの色と強度が変わります。
研究者以前の研究これに基づいて、FiberShaperの最初のバージョンを、より深いマルチモーダル代謝イメージングに適合させました。
「私たちは、このすべてのエネルギーを、私たちが望むパルス特性を持つ色に注ぎ込みたいと考えています。これにより、生成効率が向上し、組織の深部でも鮮明な画像が得られます」とCao氏は言います。
制御可能なメカニズムを構築した後、強力なレーザー光源を活用して、生体組織へのより深い浸透に不可欠なより長い波長の光を生成するイメージングプラットフォームを開発しました。
「この技術は生物学研究を大きく前進させる可能性を秘めていると信じています。これを手頃な価格で生物学研究室が利用できるようにすることで、科学者に強力な発見ツールを提供したいと考えています」とLiu氏は述べています。
ダイナミックアプリケーション
研究者がイメージングデバイスをテストしたとき、光は700マイクロメートル以上を生体サンプルに透過することができましたが、以前の最良の技術では約200マイクロメートルにしか到達できませんでした。
「この新しいタイプのディープイメージングでは、生物学的サンプルを見て、これまでに見たことのないものを見たいと考えています」とLiu氏は付け加えます。
ディープイメージング技術により、生体内の複数のレベルで細胞を見ることができ、研究者が異なる深さで起こる代謝変化を研究するのに役立つ可能性があります。さらに、イメージング速度が速いため、細胞の代謝がその動きの速度と方向にどのように影響するかについて、より詳細な情報を収集できます。
この新しいイメージング法は、臓器の構造と機能を模倣して増殖させることができる人工細胞であるオルガノイドの研究を後押しする可能性があります。Kamm研究室とGriffith研究室の研究者は、病気や治療法を評価するために臓器のように成長させることができる脳および子宮内膜オルガノイドの開発を開拓しています。
しかし、組織を切断して染色しなければ、サンプルが死んでしまうため、内部の発達を正確に見ることは困難でした。
この新しいイメージング技術により、研究者は、成長を続ける生体オルガノイドの内部代謝状態を非侵襲的に監視することができます。
これらの応用やその他の生物医学的応用を念頭に置いて、研究者たちはさらに高解像度の画像に移行することを計画しており、同時に、より少ない光でより深いイメージングを可能にすると彼らが信じている低ノイズレーザー光源の開発にも取り組んでいます。
また、画像に反応して生体試料の完全な3次元構造を高解像度で再構築するアルゴリズムの開発も行っています。
長期的には、この手法を実社会に適用し、生物学者が薬物の反応をリアルタイムで監視できるようにし、新薬の開発に役立てることが期待されています。
「組織のより深くまで到達するマルチモーダル代謝イメージングを可能にすることで、科学者は不透明な生物学的システムを自然な状態で観察する前例のない能力を提供しています。私たちは、臨床医、生物学者、バイオエンジニアと協力して、この技術の限界を押し広げ、これらの洞察を現実世界の医学的ブレークスルーに変換できることを嬉しく思います」とYou氏は言います。
「この研究は、革新的なフィードバック法を使用して、現在の技術と比較して組織のより深い細胞代謝を画像化するため、エキサイティングです。また、これらの技術は、血管内の免疫細胞の運動性のユニークな代謝動態を明らかにするために使用された高速イメージング速度を提供します。これらのイメージングツールが、ダイナミックな生命システムにおける細胞機能と代謝との関連を発見するのに役立つと期待しています」と、モーリッジ研究所の研究者で、この研究には関与していないメリッサ・スカラは述べています。
「NAD(P)H自家蛍光コントラストに頼ることで、高解像度の多光子画像をより速く、より深く組織内まで取得する能力は、さまざまな重要な問題を研究するための扉を開きます」と、タフツ大学の生物医学工学教授であるIrene Georgakoudi氏は付け加えます。「代謝機能を評価するときはいつでも、データの生理学的関連性を確保し、意味のある組織量をサンプリングし、急速な変化を監視するという点で、生体組織をできるだけ早くイメージングすることは常に大きな利点です。がん診断や神経科学のアプリケーションでは、イメージングをより深く、より迅速に行うことで、これまで生体組織で研究されていなかった疑問や相互作用をより深く探求することができます」と述べています。
この研究は、MIT Startup Funds、米国国立科学財団のCAREER賞、MITアーウィン・ジェイコブスとジョアン・クラインの大統領フェローシップ、MITカイラス・フェローシップから一部資金提供を受けています。
論文
論文:「Deep and Dynamic Metabolic and Structural Imaging in Living Tissues」
非侵襲的技術により、細胞の遺伝子発現が時間とともにどのように変化するかが明らかになる
MITの研究者は、細胞内のRNA発現を追跡して、がんの進行や胚発生などの長期的なプロセスを調査できるようになりました。アン・トラフトン | MITニュース
発行日:2024年1月10日

キャプション:この新しい方法は、生細胞の遺伝子発現の変化を長期間にわたって追跡することができます。ラマン分光法に基づくこの方法は、細胞に対して無害であり、繰り返し実行できます。
信用:画像:MITニュース;アイストック
細胞内のすべてのRNAのシーケンシングを行うと、特定の時点でのその細胞の機能と挙動について多くのことが明らかになりますが、シーケンシングプロセスによって細胞が破壊されるため、遺伝子発現の継続的な変化を研究することは困難です。
MITで開発された別のアプローチにより、研究者はそのような変化を経時的に追跡できるようになる可能性があります。この新しい方法は、ラマン分光法として知られる非侵襲的なイメージング技術に基づいており、細胞に害を及ぼさず、繰り返し実行できます。
この技術を用いて、研究者たちは、胚性幹細胞が数日間で他のいくつかの細胞型に分化するのを監視できることを示し、がんの進行や胚発生などの長期的な細胞過程の研究を可能にし、いつの日かがんやその他の疾患の診断に利用できるかもしれないことを示しました。
「ラマンイメージングにより、より多くの時点を測定できます。これは、がん生物学、発生生物学、および多くの変性疾患を研究するために重要になる可能性があります」と、MITの生物工学および機械工学の教授であり、MITレーザー生物医学研究センターの所長であり、論文の著者の1人であるPeter So氏は述べています。
MITとハーバードのブロード研究所、およびMITのポスドクであるKoseki Kobayashi-Kirschvinkは、この研究の筆頭著者であり、本日発表されましたNature Biotechnologyこの論文の筆頭著者は、元ブロードの科学者であるトンマーゾ・ビアンカラニです。Jian Shu、ハーバード大学医学部の助教授で、Broadの準会員。ジェネンテックの研究および初期開発担当エグゼクティブバイスプレジデントであるアビブ・レゲブは、ブロード大学とMITの生物学部の教員職を休職しています。
遺伝子発現のイメージング
ラマン分光法は、組織や細胞に近赤外線や可視光を当てることで、組織や細胞の化学組成を明らかにする非侵襲的な手法です。MITのレーザー生物医学研究センターは、1985年から生物医学ラマン分光法に取り組んできましたが、最近、So氏とセンターの他の人々は、ラマン分光法に基づく技術を開発しました。乳がんの診断又は血糖値を測定する.
しかし、ラマン分光法自体は、個々のRNA分子のレベルの変化のような小さなシグナルを検出するのに十分な感度ではありません。RNAレベルを測定するために、科学者は通常、シングルセルRNAシーケンシングと呼ばれる手法を使用し、組織サンプルの異なる種類の細胞内で活性のある遺伝子を明らかにすることができます。
このプロジェクトでは、MITチームは、ラマン信号をRNA発現状態に変換する計算モデルをトレーニングすることにより、シングルセルRNAシーケンシングとラマン分光法の利点を組み合わせることを目指しました。
「RNAシーケンシングは非常に詳細な情報を提供しますが、破壊的です。ラマンは非侵襲的ですが、RNAについては何も教えてくれません。そこで、このプロジェクトのアイデアは、機械学習を使用して両方のモダリティの長所を組み合わせることで、単一細胞レベルでの遺伝子発現プロファイルの経時的なダイナミクスを理解できるようにすることでした」とKobayashi-Kirschvink氏は言います。
モデルを訓練するためのデータを生成するために、研究者たちは、皮膚細胞の一種であるマウス線維芽細胞を、細胞を再プログラムして多能性幹細胞にするための因子で処理しました。この過程で、細胞は神経細胞や上皮細胞など、他のいくつかの細胞タイプにも移行できます。
ラマン分光法を使用して、研究者たちは細胞が分化する際に、18日間にわたって36の時点で細胞を画像化しました。各画像を撮影した後、研究者らは、細胞内の特定のRNA分子を視覚化するために使用できる単一分子蛍光in situハイブリダイゼーション(smFISH)を使用して各細胞を分析しました。この場合、彼らは、細胞タイプ間で発現パターンが異なる9つの異なる遺伝子をコードするRNA分子を探しました。
このsmFISHデータは、ラマンイメージングデータとシングルセルRNAシーケンシングデータとの間のリンクとして機能しました。この関連性を明らかにするために、研究者たちはまず、これらの細胞から得られたラマン画像に基づいて、これら9つの遺伝子の発現を予測するディープラーニングモデルを訓練しました。
次に、ブロード研究所で以前に開発された計算プログラムであるTangramを使用して、smFISH遺伝子発現パターンを、サンプル細胞に対してシングルセルRNAシーケンシングを実行して得られた全ゲノムプロファイルと関連付けました。
その後、研究者たちはこれら2つの計算モデルをRaman2RNAと呼ばれる1つに組み合わせ、ラマン画像に基づいて個々の細胞の全ゲノムプロファイルを予測することを可能にしました。
細胞分化の追跡
研究者らは、マウス胚性幹細胞が異なる細胞タイプに分化する際に追跡することにより、Raman2RNAアルゴリズムをテストしました:彼らは細胞のラマン画像を3日間にわたって1日4回撮影し、その後、計算モデルを使用して各細胞の対応するRNA発現プロファイルを予測し、それをRNAシーケンシング測定と比較して検証しました。
このアプローチを用いて、研究者たちは、個々の細胞が胚性幹細胞からより成熟した細胞型に分化する過程を観察することができ、また、マウスの線維芽細胞が人工多能性幹細胞に再プログラムされるときに起こるゲノム変化を2週間にわたって追跡できることも示しました。
「これは、光学イメージングが細胞の系統とその転写進化を直接追跡できる追加情報を提供することを示しています」とSo氏は言います。
研究者たちは現在、この技術を使用して、老化細胞や癌性細胞など、時間の経過とともに変化する他の種類の細胞集団を研究することを計画しています。現在、彼らは実験皿で増殖した細胞に取り組んでいますが、将来的にはこのアプローチを診断薬に発展させ、患者に使用できるようになることを望んでいます。
「ラマンの最大の利点の1つは、ラベルフリーの方法であることです。それは長い道のりですが、既存のゲノムプロファイルを測定するための侵襲的技術では不可能だった、ヒトへの翻訳の可能性を秘めています」と、MITの研究科学者で研究の著者であるJeon Woong Kang氏は述べています。
本研究は、日本学術振興会海外特別研究員、内藤財団海外特別研究員、MathWorks特別研究員、ヘレン・ヘイ・ホイットニー財団、国立衛生研究所、国立衛生研究所、国立医用画像・生物工学研究所、HubMap、ハワード・ヒューズ医学研究所、クラルマン細胞観測所の助成を受けて行われました。
イメージング法により、ヒト脳組織の新しい細胞と構造が明らかになる
高解像度イメージングを可能にする新しい顕微鏡技術は、いつの日か医師が脳腫瘍を診断し治療するのに役立つかもしれません。アン・トラフトン | MITニュース
発行日:2024年1月31日
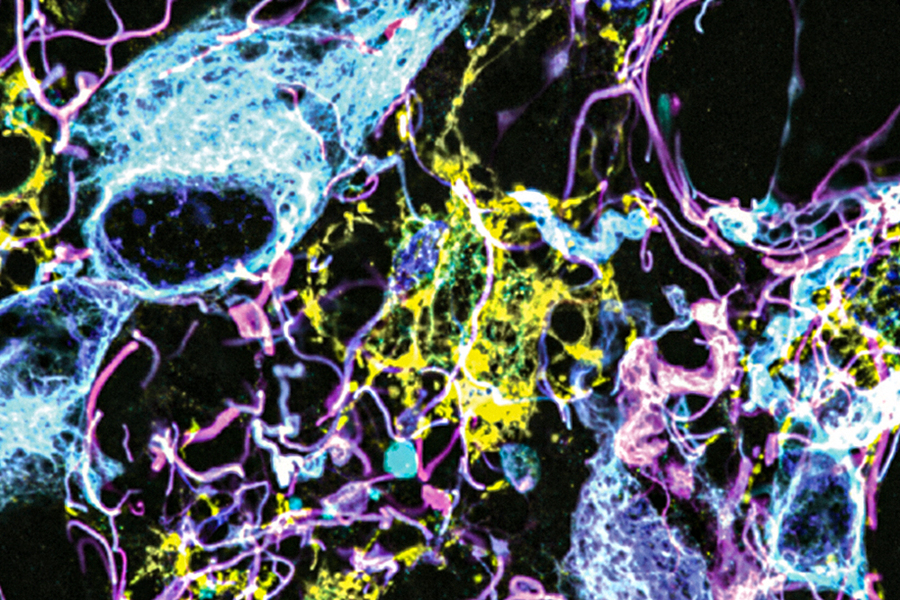
キャプション:マサチューセッツ工科大学(MIT)とハーバード大学医学部の研究者らは、新しい顕微鏡技術を用いて、ヒトの脳組織をこれまで以上に詳細に画像化しました。この低悪性度神経膠腫の画像では、水色と黄色は腫瘍に関連する異なるタンパク質を表しています。ピンク色はアストロサイトのマーカーとして使用されるタンパク質を示し、濃い青色は細胞核の位置を示します。
信用:画像:研究者提供
MITとBrigham and Women’s Hospital/Harvard Medical Schoolの研究者は、新しい顕微鏡技術を使用して、人間の脳組織をこれまで以上に詳細に画像化し、これまで見えなかった細胞や構造を明らかにしました。
彼らの発見の中で、研究者たちは、一部の「低悪性度」の脳腫瘍が予想よりも攻撃的な腫瘍細胞を含んでいることを発見し、これらの腫瘍の一部が以前に考えられていたよりも攻撃的である可能性があることを示唆しています。
研究者たちは、この技術が最終的に腫瘍の診断、より正確な予後の生成、医師の治療法選択に役立つことを望んでいます。
「私たちは、ニューロンとシナプス、および周囲の脳との間の相互作用が腫瘍の成長と進行にとってどれほど重要であるかを理解し始めています。従来のツールでは見ることができなかった多くのことが、今ではナノスケールで組織を観察し、これらの相互作用を理解しようとするツールを手に入れました」と、元MITポスドクで現在はテキサス大学医学部神経科学助教授で、この研究の筆頭著者であるPablo Valdes氏は述べています。
エドワード・ボイデン、MITの神経工学のY.エヴァ・タン教授。生物工学、メディア芸術と科学、脳と認知科学の教授。ハワードヒューズ医学研究所の調査員。MITのMcGovern Institute for Brain ResearchおよびKoch Institute for Integrative Cancer Researchのメンバー。ハーバード大学医学部の脳神経外科教授であり、ブリガムアンドウィメンズ病院の脳神経外科の学科長であるE.アントニオキオッカ。本日彼は科学トランスレーショナルメディシン。彼は、に掲載された研究の上級著者です。。
分子を見えるようにする
新しいイメージング方法は、伸縮顕微鏡これは、2015年にボイデン氏の研究室で開発された技術で、強力で高価な顕微鏡を使用して高解像度の画像を取得する代わりに、研究者たちは組織自体を拡張する方法を考案し、通常の光学顕微鏡で非常に高い解像度で画像化できるようにしました。
この技術は、水を加えると膨潤するポリマーに組織を埋め込み、通常は組織を一緒に保持しているタンパク質を柔らかくして分解することで機能します。次に、水を加えるとポリマーが膨潤し、すべてのタンパク質が互いに引き離されます。この組織拡大により、研究者は、以前は走査型電子顕微鏡などの非常に特殊で高価な顕微鏡でしか不可能だった約70ナノメートルの解像度で画像を取得できます。
2017年、ボイデン研究室は保存されたヒト組織サンプルを取得しましたを拡大する方法しかし、彼らが使用した化学試薬は、研究者が標識に興味を持っていたタンパク質も破壊しました。成長前にタンパク質を蛍光抗体で標識することで、成長プロセスが完了した後のタンパク質の位置と同一性を視覚化することができました。しかし、この種の標識に通常使用される抗体は、密集した組織が膨張する前に簡単に押し込むことはできません。
そこで、この研究では、著者らは、組織を破壊しながらサンプル中のタンパク質を保存する別の組織軟化プロトコルを考案しました。組織が拡張された後、タンパク質は市販の蛍光抗体で標識できます。その後、研究者は数回のイメージングを行い、各ラウンドで3つまたは4つの異なるタンパク質を標識できます。このタンパク質標識により、組織が拡張すると、抗体は以前はアクセスできなかったタンパク質をゼロインして標識できるため、より多くの構造をイメージングできます。
「タンパク質間のスペースを広げることで、他の方法では到達できなかった混雑した空間に抗体を取り込むことができます」とバルデス氏は言います。「組織を拡大し、タンパク質の混雑を排除し、同じ組織内の多くのタンパク質を複数回染色することでイメージングできることがわかりました。」
MITのDeblina Sarkar助教授と協力して、研究者たちは2022年にマウス組織を使用してこの形式の「クラウディングリリーフ」を実証しました。
この新しい研究は、病理学的診断と治療決定を導くために臨床現場で使用されるヒト脳組織サンプルで使用するための高密度化解除技術につながりました。これらのサンプルは通常、パラフィンに埋め込まれ、他の化学物質で処理されるため、組織が膨張する前に組織が分解されるため、取り扱いが難しい場合があります。
この研究では、研究者は組織サンプルごとに最大16の異なる分子を標識しました。彼らが標的とした分子には、軸索やシナプスなどのさまざまな構造のマーカーや、星状細胞や血管を形成する細胞などの細胞型を識別するマーカーが含まれ、腫瘍の攻撃性や神経変性に関連する分子にも標識が付けられました。
このアプローチを使用して、研究者らは健康な脳組織と、予後不良の最も侵攻性の原発性脳腫瘍である高悪性度神経膠腫と、侵攻性が低いと考えられている低悪性度神経膠腫の2種類の神経膠腫の患者からのサンプルを分析しました。
「私たちは、脳腫瘍をナノスケールでより深く理解できるように、脳腫瘍を調べたかったのです。そうすれば、将来的にはより良い治療法や診断法を開発できるでしょう。現在、神経腫瘍学では、超解像イメージングに関してあまり成果を上げていないため、それらをより深く理解するためのツールを開発する必要がありました」とValdes氏は言います。
診断ツール
彼らが研究した神経膠腫の侵攻性腫瘍細胞を特定するために、研究者たちは、非常に侵攻性の高い神経膠芽腫に見られるタンパク質であるビメンチンを標識しました。驚いたことに、彼らは低悪性度神経膠腫で他のどの方法を使用しても見たよりもはるかに多くのビメンチン発現腫瘍細胞を発見しました。
「これは、これらの腫瘍の生物学について何かを教えてくれます。具体的には、標準的な染色技術を行うことで想像するよりも攻撃的な性質を持っている可能性があるということです」とバルデスは言います。
神経膠腫患者が手術を受けると、腫瘍サンプルが保存され、免疫組織化学染色を使用して分析されるため、この研究で分析されたマーカーの一部を含む、攻撃性の特定のマーカーを明らかにすることができます。
「これらは不治の脳腫瘍であり、この種の発見により、どのがん分子を標的にすべきかを理解し、より良い治療法を設計することができます。また、ブリガム・アンド・ウィメンズ病院の臨床医がMITのエド・ボイデン氏のような基礎科学者と交流し、患者の生活を向上させる新技術を発見することの大きな影響も示しています」とChiocca氏は述べています。
研究者たちは、彼らの拡大顕微鏡技術により、医師が患者の腫瘍についてより深く知ることができ、患者の攻撃性を判断し、治療の選択を導くのに役立つことを望んでいます。バルデスは現在、この技術を使用して明らかにできる腫瘍形質に基づく診断ガイドラインを確立するために、腫瘍の種類についてより広範な研究を実施することを計画しています。
「これが、これまで不可能だったマーカー細胞や相互作用などを拾い上げる診断ツールになることを願っています」と彼は言います。「これは、神経腫瘍学および神経病理学の臨床コミュニティが、これまでにないほどナノスケールで神経疾患を見るのに役立つ実用的なツールです。なぜなら、基本的に非常に簡単に使用できるツールだからです。」
ボイデンの研究室では、この技術を使用して、健康な組織と病気の組織の脳機能の他の側面を研究することも計画しています。
「生物学は、遺伝子、遺伝子産物、ナノスケールの距離で相互作用する生体分子などのナノスケールのものを扱っているため、ナノイメージングができることは重要です」とボイデン氏は言います。「シナプスの変化、免疫相互作用、がんや老化中に起こる変化など、あらゆる種類のナノスケールの相互作用を研究することができます」
この研究は、K. Lisa Yang、Howard Hughes Medical Institute、John Doerr、Open Philanthropy、Bill and Melinda Gates Foundation、Kathy and Curt Marble Cancer Research Fund、National Institutes of Health、Neurosurgery Research and Education Foundationを通じて、Koch Institute Frontier Research Programから資金提供を受けました。
科学者の神経回路接続の視点を鮮明にする顕微鏡システム
新たに記述された技術は、2光子顕微鏡を使用して生きている脳のシナプスを画像化する際の明瞭さと速度を向上させます。デビッド・オレンスタイン | ピカワー学習記憶研究所
発行日:2024年6月18日
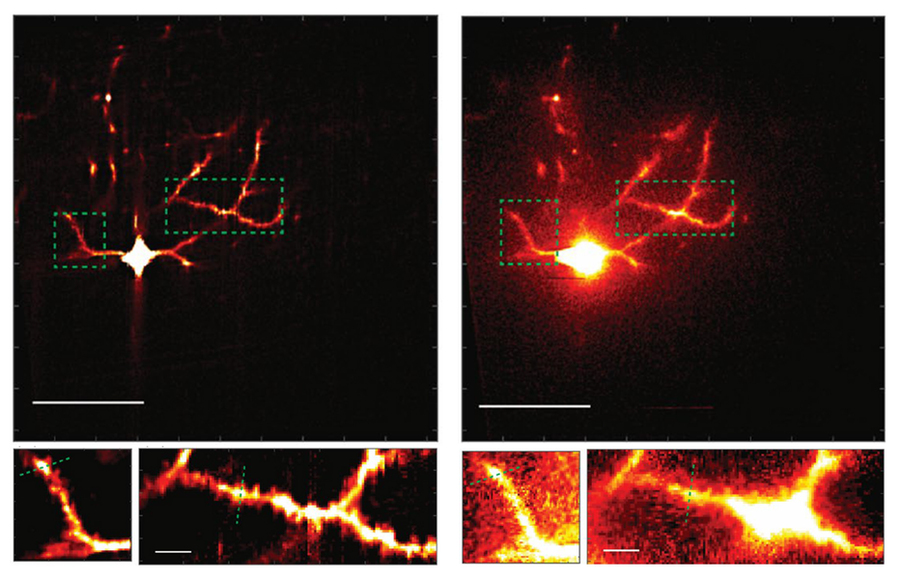
キャプション:左:多線直交走査型時間集束(mosTF)でイメージングされたニューロン。右:ライン走査型時間型集光顕微鏡(lineTF)で画像化された同じニューロン。以下は点線の領域の拡大率です。mosTF画像では、樹状突起スパインは拡大画像ではっきりと見えますが、lineTF画像ではノイズによって不明瞭になります。
クレジット:画像提供:Yi Xue, et.アル。
「マルチライン直交走査型テンポラルフォーカシング」(mosTF)と呼ばれるこのシステムは、光で脳組織のラインを垂直方向に走査することで機能します。「2光子顕微鏡」に依存する他のライブ脳イメージングシステムと同様に、この走査型光は、刺激されると蛍光を発するように設計されている脳細胞からの光子放出を「励起」します。チームのテストでは、新しいシステムは、ポイントごとに移動する2光子スコープよりも8倍高速であることが証明され、一方向にスキャンする2光子システムよりも4倍優れた信号対背景比(結果として得られる画像の鮮明さの尺度)があることが証明されました。
「生きている脳の文脈で回路構造の急速な変化を追跡することは、依然として課題です」と共著者は述べていますエリー・ネディヴィ、ウィリアムR.(1964)およびリンダR.ヤング神経科学教授ピカワー学習記憶研究所およびMITの生物学および脳および認知科学の部門。「2光子顕微鏡は、脳などの散乱組織の深部にあるシナプスを高解像度で可視化できる唯一の方法ですが、必要なポイントバイポイントスキャンは機械的に時間がかかります。mosTFシステムは、解像度を犠牲にすることなくスキャン時間を大幅に短縮します。
サンプルのライン全体をスキャンすることは、一度に1点ずつスキャンするよりも本質的に高速ですが、多くの散乱が発生します。その散乱を管理するために、一部のスコープシステムは散乱光子をノイズとして破棄するだけで、その後、それらは失われると筆頭著者は述べています李雪SM ’15、PhD ’19、カリフォルニア大学デービス校の助教授、責任著者の研究室の元大学院生ピーター・TC・ソー、MITの機械工学および生物工学の教授。新しいシングルラインおよびmosTFシステムは、散乱光子をアルゴリズムで元の位置に戻すことにより、より強い信号を生成します(したがって、刺激されたニューロンの小さくて暗い特徴を解決します)。2次元画像では、このプロセスは、1次元の単一方向システムよりも、mosTFのような2次元の垂直方向システムによって生成された情報を使用することで、より適切に達成できるとXue氏は言います。
「私たちの励起光は点ではなく線です。電球というよりは光管のようなものですが、再構成プロセスでは光子を励起線に再割り当てすることしかできず、線内の散乱を処理できません」とXue氏は説明します。「したがって、散乱補正は2D画像に対して1次元に沿ってのみ実行されます。両方の次元で散乱を補正するには、サンプルをスキャンし、もう一方の次元に沿った散乱も補正する必要があるため、直交スキャン戦略が得られます。」
この研究では、チームはポイントバイポイントスコープ(2光子レーザー走査型顕微鏡-TPLSM)とライン走査型時間集束顕微鏡(lineTF)に対してシステムを直接テストしました。彼らは、水と脂質注入溶液を通して蛍光ビーズを画像化しました。これにより、生体組織で発生する散乱の種類をよりよくシミュレートできます。脂質溶液中では、mosTFはlineTFよりも36倍優れたS/Background比で画像を生成しました。
より決定的な証拠として、Xue氏はNedivi研究室のJosiah Boivin氏と共同で、mosTFを使用して、麻酔をかけた生きたマウスの脳内のニューロンを画像化しました。脈動する血管と呼吸運動がさらなる混乱を引き起こすこのはるかに複雑な環境でも、mosTFスコープは依然として4倍優れたS/バックグラウンド比を達成しました。重要なことに、多くのシナプスが生息する特徴、つまりニューロン細胞体から伸びるつるのような突起に沿って突き出た棘または樹状突起を明らかにすることができました。ネディビ氏によると、可塑性を監視するには、これらのスパインが細胞内で成長、縮小、出入りするのを観察できる必要があります。
「ソウラボラトリー継続的な協力「顕微鏡開発における彼らの関係と専門知識により、従来の既成概念にとらわれない2光子顕微鏡ではアクセスできなかったin vivo研究が可能になりました」と彼女は付け加えます。
彼はすでにテクノロジーのさらなる改善を計画していると言います。
「私たちは、可塑性をより効果的に観察するために、より効率的な顕微鏡を開発するという目標に向けて、引き続き取り組んでいます」と彼は言います。「mosTFの速度は、高感度で低ノイズのカメラを使用する必要があるため、まだ制限されています。カメラは低速であることが多いです。私たちは現在、ハイブリッド光電子増倍管やアバランシェフォトダイオードアレイなど、より感度が高く高速な新しいタイプの検出器を備えた次世代システムに取り組んでいます。」
Xue氏、So氏、Boivin氏、Nedivi氏に加えて、この論文の他の著者はDushan Wadduwage氏とJong Kang Park氏です。
この研究は、国立衛生研究所、浜松ホトニクス、サムスン先端技術研究所、シンガポール-MIT研究技術センター、バイオシステムおよびマイクロメカニクス、ピカワー学習記憶研究所、JPB財団、ハーバード先端イメージングセンターの支援を受けました。
